서 론
마그네슘은 인체에서 네 번째로 많은 성분이며 인간의 생명 활동에 매우 중요한 역할을 하고 있다(Al Alawi et al., 2018). 하지만 최근 연구에 따르면 미국인의 45% 가 마그네슘 결핍 상태에 있는데, 이에 가장 큰 영향을 준 원인은 미국 내 농작물에 들어있는 미네랄의 양이 지난 100 년 동안 80% 이상 감소했기 때문이다(Workinger et al., 2018). 마그네슘은 인간 뿐 아니라 식물에서도 매우 중요한 역할을 하고 있다. 마그네슘은 식물에서 엽록소를 이루는 구성성분이다(Willstätter, 1915). 인체로의 마그네슘 섭취량이 줄어들거나, 체내 마그네슘 양이 줄어들게 되면, 당뇨병, 심장 관상동맥질환 및 골다공증과 같은 질병의 발생이 높아진다(Bohn, 2008). 이는 식물에서도 마찬가지로 마그네슘 흡수량이 줄어들면 식물에서도 마그네슘 부족으로 인해 생명 활동에 큰 지장을 받게 된다. 이는, 마그네슘이 식물 내에서 단백질 생성과 엽록소 합성에 관여하며(White and Broadley, 2009), 식물 내 광합성을 통한 탄소 고정과 이차 이차대사 산물 생성을 위한 효소 활동에 사용되는 매우 중요한 물질이기 때문이다(Cakmak and Kirkby, 2008; Maathuis, 2009; Hermans et al., 2013). 이처럼 마그네슘은 인간의 생명 활동뿐 아니라 식물에 있어서도 매우 중요한 역할을 하고 있기 때문에, 식물이 마그네슘을 얻을 수 있는 토양에서의 마그네슘 함량을 확인하고 관리하는 것은 지속적인 식량 생산과 공급을 위해 매우 중요한 일이다. 더불어, 전 세계적으로 인구 증가와 농촌에서 도시로의 인구 이동이 일어나고 있다(UN DESA, 2018). 이는 농촌의 노령화와 인력 부족으로 직결될 수 있다. 이 시점에서, 토양 내 마그네슘 부족으로 일어날 수 있는 농업 생산성 하락은 치명적일 수 있다. 이를 극복하기 위해 선제적으로 토양 내 마그네슘 함량을 확인하고 조절하는 기술이 필요한 시점이다.
과거 토양 내 마그네슘 함량을 분석하기 위해서는 복잡한 과정을 거쳐야 했다. 목표 지역의 토양을 샘플링하여 직접 분석하거나, 토양에서 자라는 작물을 샘플링한 뒤 작물이 흡수한 마그네슘의 양을 측정하여 간접적으로 토양 내 마그네슘을 확인하는 방법이 있다(Gransee and Führs, 2013). 두 방법 모두 다 반복이 수반되는 작업이기에 매우 노동 집약적이며, 많은 시간과 노력이 소요되고, 작업자의 숙련도에 따른 오류의 가능성도 내포하고 있다. 하지만, 이제는 기술의 발달로, Unmanned Aerial Vehicle(UAV)를 통해 획득한 항공 영상 분석을 통해 이미 자라고 있는 식물에서 생육 지수(Vegetation Index, VI)를 활용할 수 있게 되었다(Candiago et al., 2015; Kim et al., 2019). 이 방법으로는 토양을 여러 번 채취하거나, 식물을 샘플링하지 않고도 식물 내 엽록소의 양을 유추하는 것이 가능하다. 특히 Normalized Difference Vegetation Index(NDVI) 값은 식물 내 엽록소의 양과 상관관계가 매우 높은 것으로 알려져 있다(Gamon et al., 1995). NDVI의 계산 공식은 다음과 같다.
: 근적외선(NIR) 대역의 분광반사도
: 적색(RED) 대역의 분광반사도
즉, 이 공식을 통해 우리는 NDVI 값이 근적외선 대역의 분광반사도(Reflectance)와 적색 대역의 분광반사도의 비율을 통해 산출된다는 것을 알수 있다(Tucker, 1979). 엽록소에 의한 색소 흡수에 의한 적색 반사율과 세포 구조에 의한 산란으로 인산 근적외광 반사의 차이가 NDVI인 것이다(Chung et al., 2018). 즉, 건강한 식물과 스트레스 받은 식물 혹은 식물이 아닌 영역과의 구분은 가시광선영역대의 흡수율에 따라 달라지게 되며, 이는 NDVI값의 차이를 나타내게 된다. 그러므로 NDVI의 값은 식물 내 엽록소와 깊은 관련이 있다. 한편, 앞서 언급한 것처럼 마그네슘은 엽속소의 구성성분이므로 토양 내 마그네슘의 함량을 식물체 내 엽록소 함량을 통해서 유추할 수 있을 것이다(Willstätter, 1915). 그러므로 이 관계를 통해 토양 내 마그네슘 양을 비교적 정확하게 유추해 낼 수 있을 것이다.
메밀은 높은 마그네슘 함유량을 보이는 곡물이다. Ikeda et al.(2006)의 연구에 따르면, 메밀은 100 g 당 375 mg의 마그네슘을 함유하고 있는 것으로 확인되었고, 이는 같은 양의 밀, 콩 그리고 옥수수에서 보다 많은 양이다. 마그네슘은 녹황색 채소, 견과류, 곡류, 해조류 등에도 포함되어 있으며, 우리 몸에서 300개 이상 효소 활동에 관여하는 중요한 물질이며 그 섭취가 주로 음식으로 이루어진다(Al Alawi et al., 2018). 최근 100 년간 토양에서 마그네슘 부족 현상이 일어나고 있는 것이 보고되고 있다(Workinger et al., 2018). 그래서 우리는 토양에서 가장 많은 마그네슘을 흡수할 것으로 예측되는 메밀을 이용해 토양 내 마그네슘 양을 간접적으로 측정하려 한다.
우리는 이 실험을 통해, UAV 기반 메밀 밭 영상을 얻고, 이 영상을 NDVI로 분석하였다. 동시에 NDVI 값이 다를 것이라고 예상되는 메밀 밭의 여러 구역에서 메밀을 채취하여 메밀 내 엽록소의 양과 마그네슘의 양을 측정할 것이다. 최종적으로 이렇게 얻은 NDVI 값, 엽록소의 양 그리고 메밀 내 마그네슘 양과의 상호 관계를 확인하였다. 이를 통해 토양이나 식물의 직접적인 채취를 하지 않고도 쉽고 효율적으로 토양 내 마그네슘의 양을 예측할 수 있었다.
재료 및 방법
현장 실험 및 영상 획득
실험은 2018 년 제주도 서귀포시에 위치한 메밀 밭에서 진행되었다. 2018 년 10 월 14 일 DJI F550 frame을 사용하여 직접 제작한 UAV와 상용 다분광 카메라(Sequoia, France)를 사용하여 RGB 및 다분광 영상을 취득하였다. 영상은 ArduPilot Mission Planner 소프트웨어를 사용하여 85%의 전면 겹침도와 70%의 측면 겹침도를 확보한 상태로 80 m의 고도에서 2 m/s의 속도로 UAV를 자동 비행하여 촬영하였다.
영상 처리
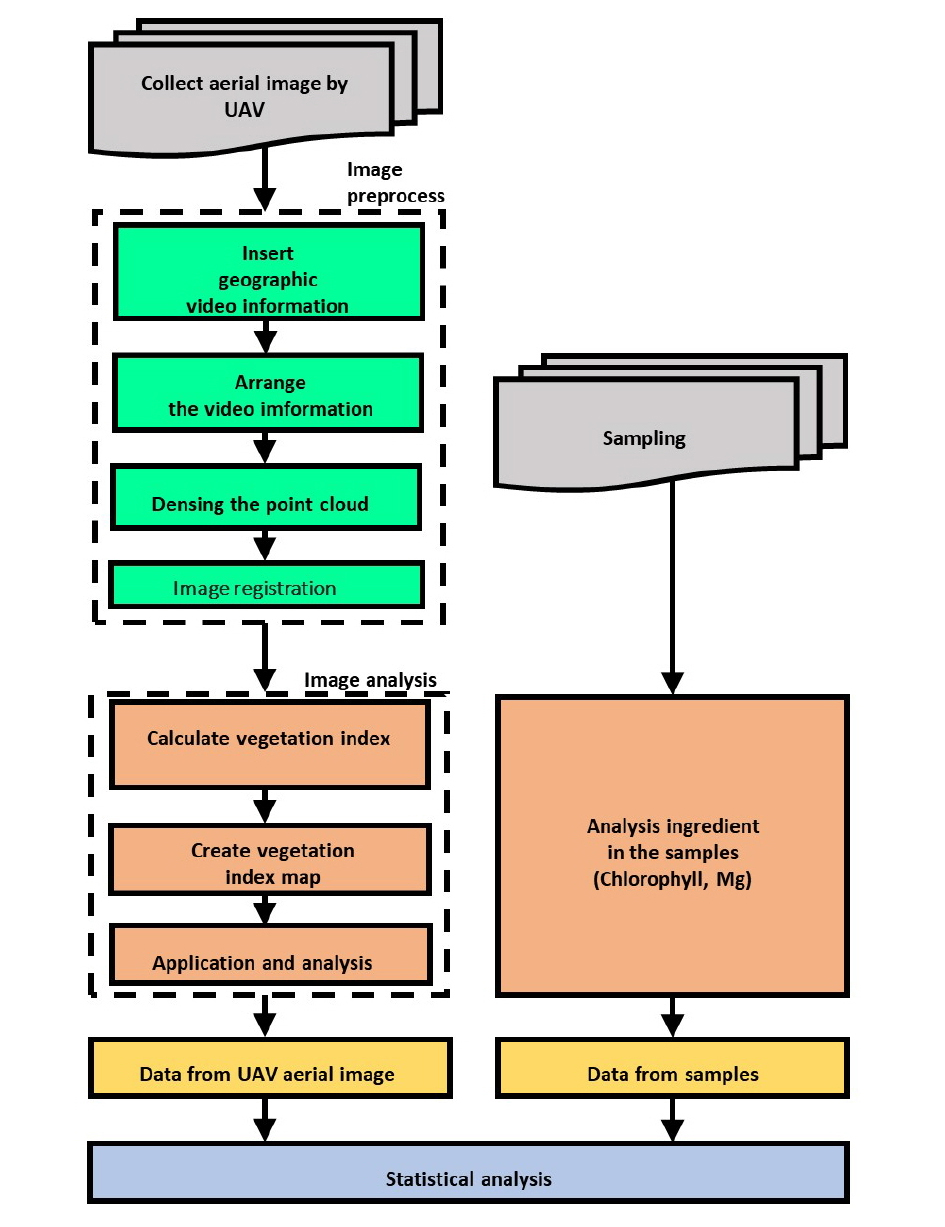
영상 정합을 위한 영상 전처리 및 분석은 Fig. 1과 같이 실시하였다. 앞서 UAV를 통해 메밀 밭의 RGB 및 다분광 영상을 획득하였다. 본 연구에서는 Pix4Dmapper Pro 3.0.17 소프트웨어를 사용하여 영상 지리정보 삽입, 영상 배열, 점구름 밀집화 과정을 거쳐 메밀 밭의 RGB 및 다분광 영상을 정합하였다.
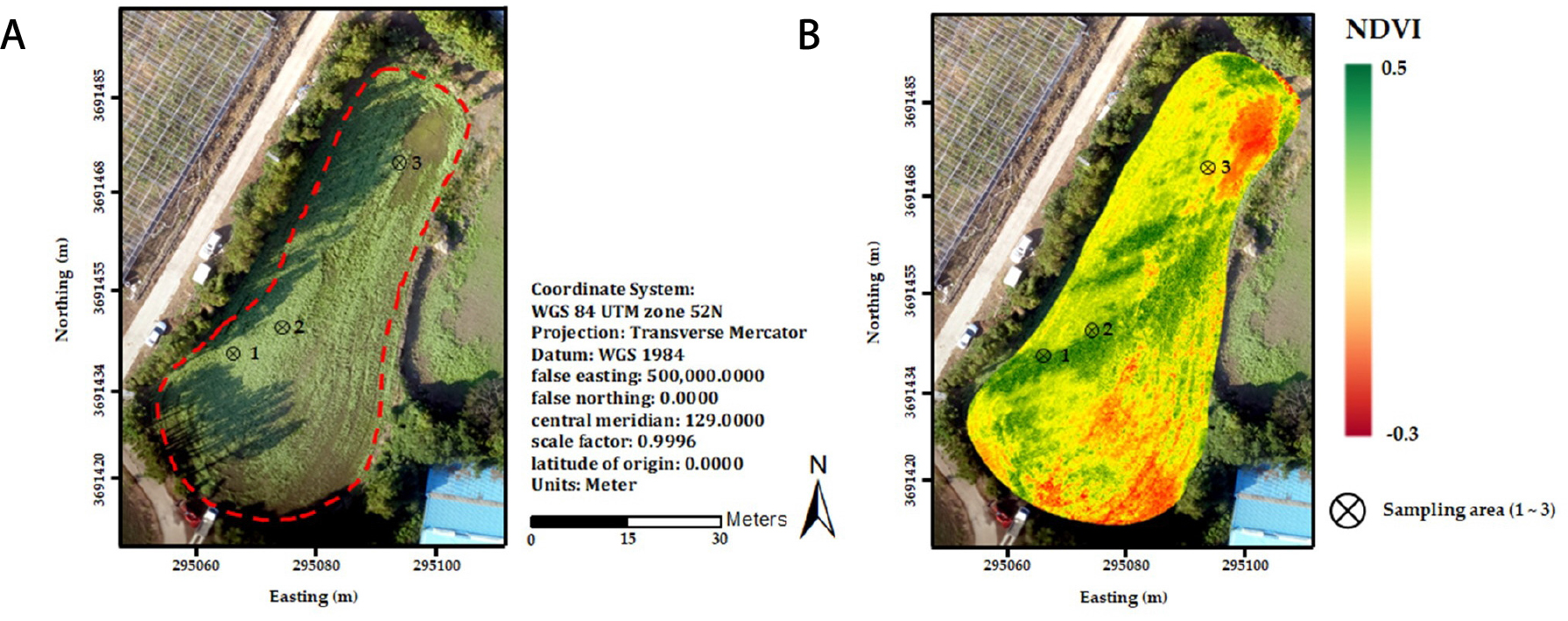
위의 과정을 통해 다양한 대역의 정합된 영상을 획득하였다. 정합된 영상을 사용하여 다양한 식생지수를 계산하고 식생지수 지도를 제작할 수 있다. 본 연구에서는 NDVI를 계산하여 NDVI 지도를 제작하였다. Fig. 2에서 영상 처리를 통해 생성된 메밀 밭의 RGB 영상(Fig. 2A) 및 NDVI 영상(Fig. 2B)을 확인할 수 있다. 그 후, 지도 내에 관심 영역을 설정하여 NDVI 값을 계산하였다.
메밀 샘플링과 분석
영상과 실측 데이터의 비교 분석을 위해, 영상을 측정한 당일에 메밀을 Fig. 2에 표시된 작물 샘플링 지역에서 채취하였다. 채취된 메밀은 실험실로 가져와서 엽록소 분석을 하고, 메밀 내 마그네슘의 양을 측정하였다.
메밀 내 엽록소는 마쇄한 시료 1 g에 80% acetone을 10 mL 첨가하여 균질화한 뒤, 10,000 g로 원심분리하여 상등액만 수집하였다. 수집한 상등액은 여과지(Watman No, 2)를 이용하여 여과한 뒤, 다시 80% acetone을 첨가한뒤, 663 nm와 645 nm 파장에서 흡광도를 측정하였다. 각 파장에서 측정한 흡광도는 다음 식을 이용하여 chlorophyll a와 chlorophyll b의 함량을 산출하였다(Porra et al., 1989).
chlorophyll a (µg/mL) = 12.15 A663 - 297 A645
chlorophyll b (µg/mL) = 21.5 A646 - 5.1 A663
메밀 내 마그네슘은 Osborne and Voogt(1978)을 이용하였다. 채취한 메밀 시료 5 g을 500°C로 가열하여 재를 얻었다. 이 재를 식힌 후 4 mL의 HNO3 용액(HNO3:H2O = 1:1)을 처리한 뒤 후드 내 hot plate 60°C에서 증발시켰다. 이를 다시 500°C로 1시간 처리하고, 6 N HCL 10 mL를 처리하여 50°C water bath에서 가열, 용해시켰다. 이것을 Whatman No. 6 거름종이로 여과해 증류수로 총량이 100 mL가 되도록 희석해 분석 시료로 하였다. 이 분석시료는 원자흡수 분광기를 사용, 마그네슘(285.2 nm)을 정량하였다.
통계 분석
통계는 R 소프트웨어를 이용하였다. 메밀 밭의 UAV 영상으로부터 얻은 NDVI 값에 대해 직접 분석을 통해 얻은 Chlorophyll a, b 전체의 양, Chlorophyll a와 b의 비율, 그리고 직접 분석을 통해 얻은 마그네슘의 양에 대해 각각 선형회귀분석을 실시하였다. 그래프는 엑셀을 이용하여 작성하였다.
결과 및 고찰
마그네슘은 동·식물 모두의 건강에 매우 밀접하게 관련되어있는 물질로, 토양 내 마그네슘 함량을 파악하는 것은 영양소가 풍부한 작물을 얻기 위해 필요하다.
NDVI를 통해 토양의 변화를 조사하려는 시도는 많이 있었다. Carvalho et al.(2014)는 NDVI값을 이용해서 토양의 침식 정도를 조사하였다. 이는 NDVI를 통해 식물의 생육 지수 뿐 아니라 다른 환경적 변화에 대한 분석도 가능하다는 것을 의미한다.
UAV를 통한 영상을 얻은 뒤, NDVI 값이 서로 다를 것이라고 예측되는 여러 구역에서 메밀을 채집하였다. Fig. 2에서 확인할 수 있듯이, 샘플 지역 1은 NDVI 값이 0.5에 가까운 녹색을 띄고 있으며, 2번 지역은 녹색과 노란색의 중간인 지역이다. 그리고 3번 지역은 노란색과 붉은색을 띄고 있는 NDVI가 -0.3에 더 가까운 지역에서 메밀을 샘플링하였다.
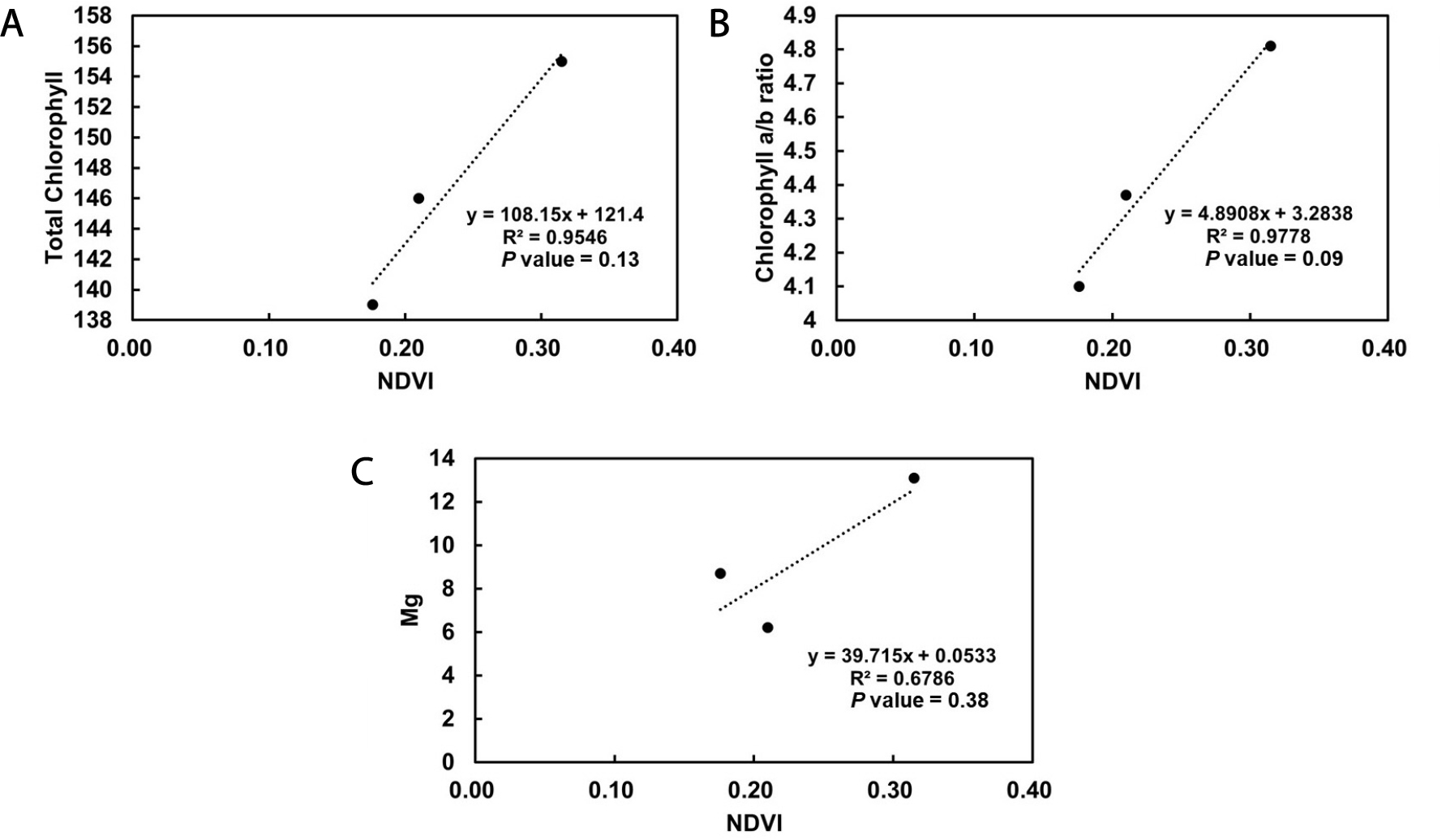
이렇게 채취한 메밀에서 엽록소 a,b의 양과 메밀 내 마그네슘의 양을 측정할 수 있었다. 이 값과 영상 처리를 통해 얻은 NDVI 값을 이용해 회귀 분석을 진행한 결과를 Fig. 3에서 확인할 수 있다. 먼저 Fig. 3A에서는 전체 엽록소의 양과 NDVI값이 양의 계수를 가지며, R2 값이 0.9546이고, P값은 0.13으로 나타난다. P값이 0.05보다 크므로 유의하다고 볼 수 없는 값이나, 이는 NDVI의 측정만으로도 메밀 내 엽록소의 양을 예측할 수도 있음을 나타낸다. Fig. 3B에서 볼 수 있는 엽록소 a와 b의 비율에서도 마찬가지 결과를 보여주고 있다. 엽록소 a와 b의 비율에서 R2 값은 0.9978이고, P값은 0.09로, P값이 더 작으므로 NDVI는 전체 엽록소의 양보다는 유의하게 엽록소 a와 b의 비율을 예측할 수 있음을 보여주고 있다. 하지만 역시, P값이 0.05보다 큰 값으로 통계적으로 유의하지는 않다. 마지막으로 Fig. 3C에서 NDVI와 마그네슘의 양을 회귀분석한 결과를 보면, 양의 계수를 가지며, R2 값은 0.6786이고 P값은 0.38로 가장 유의하지 못하게 나타내고 있다. 하지만 엽록소의 필수 구성요소가 마그네슘인 것을 감안할 때 UAV영상을 통한 마그네슘 함량 예측은 가능할 것이다.
NDVI로 마그네슘의 양을 효율적으로 예측할 수 있다는 것이 확실히 증명되려면 더 많은 연구결과가 뒷받침되어야 하겠으나, 이 실험을 통해서 NDVI를 통해서 토양 내 마그네슘의 양을 유추할 수 있는 가능성이 존재한다는 사실을 확인할 수 있었다. 이 방법은 UAV를 통한 항공 사진을 이용하기 때문에 반복 측정이 용이하고, 결과를 금방 확인할 수 있다는 장점을 지닌다. 또한, 노동 집약적이며 분석 시험에 숙련된 인적 자원을 필요로 하고 분석에 많은 시간을 요구하는 직접 분석에 비해 숙련되지 않은 인원이 쉽게 토양 내 마그네슘의 양을 확인할 수 있다는 장점도 있다.
하지만, 어디까지나 간접적인 측정법이라는 한계점이 있고, 토양에서 직접 마그네슘의 양을 측정하는 것이 아닌, 토양에서 자란 식물에게서 간접적으로 측정하는 방법이기 때문에, 식물이 없는 땅에서는 마그네슘의 양을 측정할 수 없고, 식물의 최대 흡수량까지만 마그네슘을 측정할 수 있다는 단점을 지닌다. 메밀은 곡물 중 마그네슘 함량이 높은 작물로 알려져 있어(Ikeda et al., 2006), 토양에서 흡수할 수 있는 마그네슘의 양이 높을 것으로 생각된다. 그러므로 토양 내 마그네슘의 양을 간접적으로 측정할 때, 최대치를 높게 설정할 수 있는 작물이므로 간접적으로 측정하는 데 있어서 발생하는 단점을 일부분 상쇄할 수 있을 것이다.
앞으로의 연구에서는 마그네슘 흡수와 저장률이 더 높은 식물을 발굴해내어 토양 내 마그네슘의 양을 간접적으로 측정할 수 있는 방법을 좀 더 구체화시키고, 다양한 토양에서 시험하여 정교한 측정 방법을 정립해야 할 것이다.
요 약
토양의 마그네슘 결핍이 작물 생산성 감소를 불러일으키고, 마그네슘이 결핍된 작물을 섭취한 인간의 건강까지 위협하고 있다. 전 세계적으로 인구는 증가하고 있는 데 비해, 농촌 인력이 감소하고 더 많은 농작물을 소비하는 도시인구는 증가하는 추세이다. 이렇게 변화하는 인구 구조에도 불구하고 안정적으로 식량을 공급하기 위해서 토양내 마그네슘 양을 확인하고 조절하는 기술이 요구되고 있다. UAV 항공 이미지 분석을 사용하여 식물 내 마그네슘을 예측할 수 있다. 이를 통해서 토양의 마그네슘 양을 예측할 수 있을 것이다. 이 연구에서는 UAV를 사용하여 메밀밭의 영상을 수집하였다. 그 영상을 생육지수로 분석하여 생육 지수를 확인함과 동시에 메밀을 샘플링하여 메밀 내 엽록소와 마그네슘의 양을 측정하였다. 우리는 생육지수 중에서 NDVI를 사용하였는데, 이 생육 지수는 식물의 엽록소 함량과 높은 상관 관계가 있다. 또한, 식물 내 엽록소는 마그네슘을 필수 성분으로 한다. 회귀 분석 결과 총 엽록소와 NDVI 값은 양의 상관 계수를 가지며 R2 = 0.9546 이었다. 또한 메밀과 마그네슘 함량은 회귀분석 결과 양의 상관 계수를 가지며, R2 = 0.6786 이었다. 이 사례 연구를 발전시켜 나간다면, 토양 내 마그네슘 양을 예측하는 보다 쉽고 효율적인 방법을 찾을 수 있을 것이다.