서 론
앱시스산의 기능
앱시스산 신호전달과정을 통한 환경스트레스 방어반응
기공 개폐에 관여하는 앱시스산 신호전달과정
앱시스산 신호전달과정에서 앱시스산 수용체(receptor)의 역할
앱시스산 신호전달 과정에서 SnRK2 인산화효소와 A-그룹 PP2C 탈인산화효소의 기능
앱시스산 신호전달 과정에서 SnRK2 인산화효소와 PP2C 탈인산화효소의 상호작용
앱시스산 신호전달과정에서 이온 채널 및 기공 개폐 조절
결 론
서 론
최근에 나타나고 있는 기후변화로 인한 지구 온난화 현상은 오랜 동안 지속되어 오던 농업 환경 및 농생태계의 변화를 초래하는 주요 요인으로 부상하고 있다. 식물은 자연 및 농생태계 환경에서 끊임없이 생물적/비생물적 스트레스에 노출되어 있다. IPCC (Intergovernmental Panel on Climate Change, 2007)는 지난 100년간 지구의 평균기온이 0.74°C 상승하였고 2100년에는 1999년 대비 최대 6.4°C까지 상승할 것으로 전망하고 있다. 국내의 경우 지난 100년간 평균 기온이 1.5°C 상승하여 세계적인 상승세에 비하여 그 변화의 폭이 크다. 또한 농업에 중요한 요소인 강우량의 경우에도 최근 10년간 평년 대비 10% 증가하고 있으나 시기적으로 일시적인 가뭄이 나타나는 등 기후변화가 심화되고 있다.
식물은 스트레스를 회피하지 못하는 특성으로 인하여 기후변화에 대하여 더 많은 스트레스를 받고 있고 이로 인하여 스트레스에 대한 방어 기작이 잘 발달되어 있다. 스트레스에 대한 식물의 반응은 다양한 방법으로 나타나고 있는데 가장 대표적으로 식물 호르몬인 앱시스산(abscisic acid, ABA)이 잘 알려져 있다. 최초로 앱시스산이 발견된 것은 1960년대이고 이 발견에 대한 화학적, 생물학적 재검토는 각각 1969년과 1974에 이루어졌다(Addicott and Lyon, 1969; Moes et al., 2008). 미국 농무부(USDA)의 Addicott 그룹은 낙엽현상을 촉진하는 물질을 목화에서 추출한 화합물에서 찾고 있었는데, cotyledon abscission assay를 이용하여 이와 관련된 물질을 찾아내었다(Ohkuma et al., 1963). 처음 분리되었을 때 이 화합물은 abscisinII로 명명되었고 이 물질의 기능 분석을 통하여 이 물질의 처리에 의해 엽초 성장이 억제되는 것이 확인되었다(Cracker and Abeles, 1969). 플라타너스 잎의 추출물에 존재하는 dormin이라는 물질이 밀의 발아를 억제하는 물질로 분리되었고 이 물질이 식물의 생장억제 효과를 나타내었는데 화학분석을 통하여 dormin과 abscisinII가 똑같은 화합물이라는 것을 확인하였다(Cornforth et al., 1965). 지난 30년 동안, 분자생물학 및 생화학 연구를 통하여 앱시스산 신호전달에 관련된 100개의 loci와 2차전달자를 밝혀내었는데, 여기에는 Ca2+, 활성산소(reactive oxygen species, ROS), cyclic nucleotides와 phospholipids가 관여한다고 알려져 있다.
이 총설에서는 환경스트레스와 관련된 식물의 반응을 세포내에서 앱시스산 신호전달 과정에 초점을 맞추어 기술하였다. 특히 최근에 가장 연구가 많이 되고 있으며 앱시스산 신호전달요소로 알려져 있는 앱시스산 수용체로부터 실질적으로 반응을 나타내는 이온채널까지의 경로를 분자생물학적, 유전학적, 생리학적 관점에서 논의하였다.
앱시스산의 기능
앱시스산의 식물에서의 생리학적 효과는 앱시스산의 발견 이후에 검증되었다. 식물의 발아와 α-amylase 합성 유도에 관여하는 식물 호르몬 지베렐린(gibberellin)에 상반되는 효과를 가지는 앱시스산의 기능을 밝혔고 특히 공변세포 반응에서 수분생리에 앱시스산이 역할 한다는 것을 돌연변이 식물체를 이용하여 밝혔다(Thomas et al., 1970). 이 돌연변이체의 경우 앱시스산 합성이 일어나지 않는 식물체로서 스트레스 상황에서 앱시스산의 결핍이 나타났고 이로 인하여 기공이 닫히지 않아 물의 손실이 많아지게 되어 시들음 현상이 나타났다. 또한 이 식물체에 앱시스산을 처리하면 기공 폐쇄가 유도되어 시들음 증상이 회복되었다(Illingworth et al., 2008; Tal et al., 1970). 이러한 연구를 토대로 앱시스산이 공변세포(guard cell) 개폐를 조절하는 핵심적인 역할을 한다는 생리학적 모델이 1970년대 초반에 제시되었고 건조스트레스와 관련하여 앱시스산의 역할은 광범위하게 연구되고 재검토되었다(Nilson and Assmann, 2007; Schroeder et al., 2003; Sirichandra, 2009). 일반적으로 수분이 부족한 상황에서는 식물 지상부의 생장이 멈추게 되지만 앱시스산의 작용에 의해 뿌리 생장은 계속 유지되는 것이 밝혀졌다(Sharp et al., 2004). 물론 이 모든 과정이 앱시스산 단독으로 조절되는 것이 아니라 다른 여러 가지 호르몬이 관여하는 복잡한 신호전달경로에 의해 제어되지만 그 중에서 앱시스산의 역할이 가장 크다고 할 수 있다. 식물체내에서의 수분의 균형이 잡히지 않을 경우, 다양한 기작들이 앱시스산과 다른 호르몬들의 신호전달과정을 통하여 스트레스 반응 유전자의 발현을 조절하게 되고 이를 통하여 탈수를 회피하거나 견뎌내기 위한 기작들이 작동 된다(Zhu, 2003). 특히, 화합성 용질(compatible solute)의 축적, dehydrins과 LEA 단백질 등의 합성은 스트레스 상황에서 수분유지와 단백질의 변성을 막는 두 가지 중요한 역할을 수행하게 된다. 최근에 앱시스산이 병원균의 감염에 영향을 미친다는 것이 알려 졌다. 앱시스산은 기공 폐쇄를 유도하여 기공을 통한 세균성병원균의 출입을 통제하여 병 저항성에 역할을 하기도 하고 살리실산(salicylic acid)과 같은 병 저항성을 유도하는 호르몬들과의 상호작용을 거쳐 방어 기작을 방해하여 식물을 감수성으로 만드는데 역할을 하기도 한다(Anderson et al., 2004; Asselbergh et al., 2008; Lim et al., 2014; Melotto et al., 2006, 2008; Mosher et al., 2010; Ton et al., 2009).
앱시스산은 식물의 생물적(biotic) 스트레스와 무생물적(abiotic) 스트레스 반응에서 뿐만 아니라 식물성장과 발달, 배아와 종자의 발달, 내건성과 휴면의 촉진, 발아, 어린식물의 자립 같은 일들에 관여한다. 앱시스산의 생합성에 심한 결함이 있거나 앱시스산의 무감각 돌연변이의 경우 수분환경이 양호한 상태에서도 발육이 정지되는 표현형을 보여주고 종자 생산이 악화되었다(Barrero et al., 2005; Cheng et al., 2002; Fujii and Zhu, 2009; Nakashima et al., 2009).
앱시스산의 구조가 여러 연구를 통해 제시되었고 이 분자구조가 식물의 생물학적 기능에 중요한 특성을 가지고 있다는 것이 밝혀졌다(Cornforth et al., 1965; Ohkuma et al., 1965). 앱시스산의 입체중심이 중요하다는 것은 R(‒)-앱시스산과 S(+)-앱시스산의 생물학적 특성을 연구하여 밝혀졌다(Rin et al., 2005; Zaharia et al., 2005). 기공의 개폐 등에 대한 많은 연구에서 R(‒)-앱시스산은 S(+)-앱시스산에 비해 활성이 약하다고 알려졌다. 벼(Walker-Simmons et al., 1992) 및 애기장대(Nambara et al., 2002)의 종자 발아 연구에서 R(‒)-앱시스산이 S(+)-앱시스산과 다른 기능을 가지고 있는 것이 확인되었고(Lin et al., 2005), 애기장대에서 앱시스산에 대한 최근의 microarray 연구에서 R(‒)-앱시스산이 대부분의 S-(+)-앱시스산에 의해 조절되는 유전자를 다시 조절한다는 것을 보여 주었다(Huang et al., 2007). 유전학적 연구는 애기장대 종자의 R(‒)-앱시스산의 기능이 앱시스산 신호전달 경로를 필요로 한다는 것을 보여주었고 R(‒)-앱시스산 및 S(+)-앱시스산을 받아들이는 두 가지 수용체가 각각 존재한다고 밝혀졌다(Nambara et al., 2002). 최근에 발견된 PYR/PYL/RCAR 앱시스산 수용체 family가 양쪽 입체이성질체에 결합하는 것이 밝혀졌다(Ma et al., 2009; Park et al., 2009).
앱시스산 신호전달과정을 통한 환경스트레스 방어반응
앱시스산은 종자의 발아, 식물의 생장 및 발달 그리고 생물적 및 무생물적 스트레스에 대한 중요한 반응들을 조절한다. 특히 건조과 같은 무생물적 스트레스는 앱시스산 합성을 유도하며, 이것은 스트레스 관련 유전자의 발현이나 기공폐쇄 같은 잘 알려진 분자적이고 세포수준에서의 반응을 유도한다. 최근까지의 연구를 통하여 앱시스산 신호전달과 관련된 구성요소가 확인되었고 구성요소간의 상호작용 및 서로 간의 관계가 상세히 분석되고 있다. 앱시스산 신호 전달에 대한 연구 중 앱시스산의 수용체에 대한 규명과 앱시스산 신호를 세포의 반응으로 이끄는 후속의 신호전달 과정이 확인되었는데 특히 앱시스산과 이들의 신호를 인식하는 PYR/PYL/PCAR 수용체, 이 수용체에 의해 불활성 되는 2C-type 탈인산화효소의 작용과 SnRK2-type 인산화효소 작용 및 이들의 상호작용에 의한 공변세포의 이온채널의 활성화와 기공의 개폐로 이어지는 연구가 활발히 이루어지고 있다(Ma et al., 2009; Park et al., 2009).
기공 개폐에 관여하는 앱시스산 신호전달과정
식물에 영향을 미치는 다양한 스트레스 중 건조는 식물의 생장에 가장 크게 영향을 미친다. 식물은 생장 및 발달 궁극적으로는 생존을 위해 광합성 기작을 수행해야 하고 이를 위해 이산화탄소의 공급이 이루어져야 하는데 이는 대부분 잎에 있는 기공을 통하여 일어난다. 이러한 이산화탄소의 공급은 수분의 손실을 야기하는데 일반적으로 한 분자의 이산화탄소를 수급하기 위하여 식물의 기공에서는 많은 양의 물 분자를 공기 중에 내어 놓아야 한다. 이러한 이유 때문에 수분 공급은 식물 생장을 제한하는 중요한 요인으로 작용을 하게 되고 건조 스트레스는 심각한 식물 생산 감소를 초래한다. 앱시스산은 식물호르몬 중 수분의 상태와 기공의 기능을 조절하는 주요한 호르몬이다. 건조한 조건에서 식물은 기공 폐쇄를 유도하는 앱시스산을 생합성(biosynthesis)하고 축적하여 증산작용을 억제하고 이는 결과적으로 수분손실을 방지하게 해준다. 앱시스산에 의한 기공 폐쇄를 기반으로 하는 세포수준의 분자기작은 널리 연구되고 있다(Assmann 2003; Cutler et al., 2010; Hubbard et al., 2010; Lim and Lee, 2006; Lim et al., 2017; Luan 2002; Popko et al., 2010; Wasilewska et al., 2008; Wilkinson and Davies 2010). 일반적으로, 앱시스산 수준은 앱시스산의 생합성과 앱시스산 분해 작용의 균형에 의해 조절 된다(Nambara and Marion-Poll 2005; Nilson and Assmann 2007). 여러 연구를 통하여 9-cis epoxycarotenoid dioxygenase (NCED) 유전자들이 앱시스산의 생합성에 중요한 효소를 암호화 한다는 것이 밝혀졌다(Schwartz et al., 1997; Tan et al., 1997; Thompson et al., 2000). 건조한 환경 조건에서 AtNCED3 유전자의 발현이 강하게 유도 되었고 AtNCED3 단백질의 분해는 앱시스산의 생합성을 억제하여 앱시스산의 수준을 감소시키며 이 유전자가 발현되지 않는 돌연변이체(knock-out mutant)는 앱시스산의 축적이 일어나지 않아 애기장대에서 높은 증산율을 보이는 표현형을 나타낸다(Iuchi et al., 2001). 이와는 대조적으로 NCED유전자가 과발현(overexpression)되면 높은 수준의 앱시스산 축적과 낮은 증산율을 나타내게 되고 이로 인하여 건조와 같은 여러 환경스트레스에 대하여 내성의 표현형을 보이게 된다(Iuchi et al., 2001; Schwartz et al., 1997; Schwartz et al., 2003; Tan et al., 1997; Thompson et al., 2000). 이화작용에서, 8‘-hydroxylase를 암호화하는 CYP707 유전자들은(CYP707A1~CYP707A4) 앱시스산 분해에 중요한 역할을 한다(Kushiro et al., 2004; Umezawa et al., 2006). CYP707A3 유전자가 발현되지 않는 돌연변이체(cyp707a3-1)는 높은 수준의 앱시스산 함량을 나타내고 이에 따라 낮은 증산율을 보여 건조에 대한 저항성 표현형을 보였다(Umezawa et al., 2006).
기공 개폐조절에서 공변세포의 팽압은 K+채널과 음이온 채널을 통한 이온 유입 및 배출에 의해 조절 된다. 공변세포에서의 이러한 이온 채널들은 광합성과 관련되어 있는 빛, CO2 농도와 건조 등과 같은 스트레스 그리고 기타 수많은 환경요인에 의하여 조절된다. 건조와 같은 환경스트레스의 경우 앱시스산은 주요한 신호로 작용하여 활성산소, Ca2+같은 이차 전달자를 통해 기공을 폐쇄시키는데 이 과정은 이온 채널을 기질로 사용하는 단백질 인산화효소(protein kinase)/탈인산화효소(protein phosphatase)의 활성화와 불활성화에 의해 조절 된다(Chen et al., 2010; Garcia-Mata and Lamattina, 2001, 2003; Grabov and Blatt, 1998, 1999; Hamilton et al., 2000; Lee et al., 2009; Negi et al., 2008; Pei et al., 2000; Schroeder and Hagiwara, 1989; Sokolovski et al., 2005; Vahisalu et al., 2008, 2010; Ward et al., 2008). 앱시스산을 인식하는 단계에서 기공 폐쇄까지의 신호전달과정의 가장 최근 모델은 다음 부분에서 논하려 한다.
앱시스산 신호전달과정에서 앱시스산 수용체(receptor)의 역할
이전의 많은 연구를 통하여 식물의 주요 호르몬에 대한 수용체(receptor)가 밝혀졌는데 앱시스산 수용체의 경우에는 1개 이상의 앱시스산 수용체가 존재할 것이라고 제안되었다(Kitahata et al., 2005; Pedron et al., 1998; Zhang et al., 2001). 현재까지 다양한 앱시스산 수용체가 제시 되었는데 많은 앱시스산 수용체로 제시된 단백질들이 식물에서 수용체가 아닌 다른 기능을 하고 있다고 밝혀졌다(Christmann and Grill, 2009; Liu et al., 2007; Ma et al., 2009; Park et al., 2009; Pandey et al., 2009; Shen et al., 2006). 앱시스산 조절과 관련되어 있는 2C type의 탈인산화 효소(PP2C)나 SnRK2-type 단백질 인산화효소와 기능적으로 연결되어 있는 pyrabactin 저항성(PYR)-like (PYL)/RCAR 단백질 그룹의 앱시스산 수용체들이 밝혀지면서 앱시스산의 신호전달 과정에 관련되어 있는 연구가 최근에 많이 이루어지고 있다(Ma et al., 2009; Park et al., 2009).
PYR/PYL/RCAR 앱시스산 수용체는 star-related lipid-transfer (START) 단백질 그룹에 속해 있으며 Bet v 단백질과 상동성을 가지고 있다(Ma et al., 2009; Park et al., 2009; Santiago et al., 2009b). Park 등(2009)은 pyrabactin이라는 앱시스산 유사체를 사용하여 돌연변이체를 screening하는 방법으로 PYR/PYL을 암호화하는 유전자들을 분리하였다고 Ma 등(2009)은 PP2C 중 하나인 ABI2와 상호작용하는 단백질을 찾는 방법으로 RCAR을 규명하였다. 이 두 가지 경우에서, 앱시스산이 PYR/PYL/RCAR 단백질과 직접적으로 결합한다는 것이 밝혀졌고 이에 따라 앱시스산의 수용체로써 역할을 할 것이라고 제안 되었다. 그러나 이 유전자의 발현이 억제된 돌연변이체(pyr1)의 경우 앱시스산에 대하여 어떠한 표현형도 보이지 않았는데 이것은 아마도 PYR/PYL/RCAR 단백질 family가 14개의 member를 가지고 있기 때문일 것이라 생각되어 졌고(Nishimura et al., 2010; Park et al., 2009) 이들 유전자 중 세 개(pyr1:pyl1:pyl4) 및 네 개(pyr1:pyl1:pyl2:pyl4)의 유전자가 변이된 돌연변이를 사용하여 유전학적 분석을 수행한 결과, 이 돌연변이체들의 발아, 뿌리 생장 그리고 기공 폐쇄에서 앱시스산에 대하여 감수성이 줄어드는 것이 확인 되었고 이를 통해 이들 유전자들이 앱시스산 신호전달 과정에서 역할을 한다는 것을 규명할 수 있었다.
A 그룹의 PP2C의 경우 앱시스산 신호전달 과정에서의 음성조절자(negative regulator)로서 역할을 한다고 알려져 있다(Gosti et al., 1999; Merlot et al., 2001; Schweighofer et al., 2004; Wasilewska et al., 2008). PYR/PYL/RCAR 단백질이 in vitro 상에서 직접적으로 PP2C 탈인산화효소와 상호작용을 하고 효소활성을 억제한다고 알려졌다. PYR/PYL/RCAR과 탈인산화효소와의 상호작용은 두 가지 방법으로 이루어진다는 것이 밝혀졌다. 첫째로, PYR/PYL/RCAR 단백질의 앱시스산 결합자리에서 중요한 역할을 하는 리간드(ligand) 결합 위치가 존재하고, PYR/PYL/RCAR과 상호작용하는 PP2C 사이의 몇몇 상호작용들이 앱시스산에 의해 강화된다(Melcher et al., 2009; Miyazono et al., 2009; Nishimura et al., 2009; Santiago et al., 2009a; Yin et al., 2009). 두 번째로는 이와는 반대로 다른 상호작용들은 앱시스산 비의존적으로 PP2C와 결합한다(Ma et al., 2009; Santiago et al., 2009b). 이 두 가지 모델들이 PYR/PYL/RCAR 복합체에서 앱시스산의 기능을 설명할 수 있다. 한 가지는 앱시스산과의 결합이 PYR/PYL/RCAR의 구조적 변화를 유발하고 앱시스산과 결합한 PYR/PYL/RCAR 수용체는 PP2C와 단단히 상호작용을 할 수 있다는 것이다. 다른 한가지는 앱시스산이 어떤 단백질의 구조에도 영향을 미치지 않고 오직 PYR/PYL/ RCAR-PP2C 복합체에만 결합한다는 것이다. PYR1, PYL1, PYL2의 구조적 분석을 통하여 PYR/PYL/RCAR이 앱시스산과 결합하고 PP2C를 인식하는 표면을 만들어 PP2C와 복합체를 형성한다는 것을 보여주고 있다(Melcher et al., 2009; Miyazono et al., 2009; Yin et al., 2009). 이 복합체에서 앱시스산과 결합한 PYR/PYL/RCAR은 PP2C의 활성부위와 상호작용하여 PPC2의 활성부위가 다른 기질과의 상호작용을 억제함으로서 탈인산화 효소로서의 활성을 저해한다. 또한 PP2C의 트립토판(tryptophan) 잔기는 ABA-PYR/PYL/RCAR-PP2C 복합체를 안정화시키고 앱시스산과의 결합을 용이하게 한다(Melcher et al., 2009; Miyazono et al., 2009; Yin et al., 2009). 이 결과들은 다양한 A 그룹의 PP2C의 불활성화가 앱시스산과 앱시스산 수용체인 PYR/PYL/RCAR에 의해 조절된다는 것을 의미한다(Ma et al., 2009; Park et al., 2009; Santiago et al., 2009b; Szostkiewicz et al., 2010). 이러한 유전적, 생리적, 구조적 분석을 통하여 현재까지 알려진 다양한 앱시스산 수용체 중 PYR/PYL/RCAR가 실질적으로 앱시스산 수용체로서 기능을 수해하고 있다는 것을 말해 주고 있다.
앱시스산 신호전달 과정에서 SnRK2 인산화효소와 A-그룹 PP2C 탈인산화효소의 기능
앱시스산 신호전달과정에서 단백질의 인산화와 탈인산화는 다른 신호전달 과정과 마찬가지로 중요한 과정이며 이는 몇몇 단백질 인산화효소(protein kinase) 및 탈인산화효소(protein phosphatase)와 관련되어 있다고 알려져 있다(Lee et al., 2009; Vlad et al., 2009; Geiger et al., 2009). 처음으로 보고된 SnRK2-type의 인산화효소는 밀에서 분리된 PKABA1이다(Anderberg et al., 1992). PKABA1의 활성은 앱시스산에 의해 유도되고 이 단백질의 활성은 TaABF1의 인산화와 관련 되어 있고(Anderberg et al., 1992; Johnson et al., 2002) 이 전사인자는 앱시스산에 의해 유도되는 유전자의 발현을 억제하는 것이 밝혀졌다(Gomez-Cadenas et al., 1999; Johnson, Shin and Shen, 2008). 후속연구를 통하여 앱시스산에 의해 활성화되는 세린(serine)-쓰레오닌(threonine) 단백질 인산화효소(AAPK)가 자두에서 확인되었다(Li et al., 2000). AAPK는 SnRK2-type의 인산화효소이며 세포막의 음이온 채널(slow-type anion channel (SLAC))의 조절을 통한 기공 폐쇄와 연관되어 있다고 밝혀졌다(Li et al., 2000). 애기장대에서 이 AAPK와 상동성이 있는 단백질이 유전학적 방법에 의해 밝혀 졌는데 SnKR2-type의 인산화효소인 OST1 (Open Stomata 1, SnRK2.6)으로 확인되었다(Mustilli et al., 2002). OST1의 경우 앱시스산에 의해 발현이 조절이 되지 않지만 인사화효소의 활성이 조절되는 특징을 가지고 있다(Mustilli et al., 2002;Yoshida et al., 2002). ost1 돌연변이체는 앱시스산에 둔감한 표현형을 보여주었고 건조한 조건에서 조차도 기공이 개방되어 있어 수분 손실이 야생종에 비해 컸다(Mustilli et al., 2002;Yoshida et al., 2002). 또한 OST1은 앱시스산에 의해 발현되는 전사인자인 ABRE을 인산화시키고 앱시스산 조절 유전자의 발현을 조절하는 다른 전사인자인 ABF2, ABF3도 인산화시키는 것이 확인되었다(Fujita et al., 2009; Furihata et al., 2006; Sirichandra et al., 2010). OST1과 더불어 SnRK2 type 인산화효소인 SnRK2.2와 SnRK2.3는 OST1 유전자와는 다르게 앱시스산에 의해 유도되고 인산화활성도 조절되며 이들도 각각 앱시스산 신호전달 과정에서 기능을 한다는 것이 밝혀졌다(Boudsocq et al., 2004). snkr2.2/snrk2.3 이중 돌연변이(double mutant)는 종자의 발아와 뿌리의 성장에서 앱시스산에 둔감한 표현형을 나타내는 반면에 각각의 단일 돌연변이는 기능적 중복성(redundancy) 때문에 별다른 표현형을 나타내지 않는다(Fujii et al., 2007). 이들의 삼중 돌연변이(snkr2.2/snrk2.3/누가2.6)는 앱시스산 신호전달의 과정이 이루어지지 않아 건조 스트레스에 대해 아주 높은 감수성 표현형을 나타낸다(Fujii and Zhu, 2009; Fujita et al., 2009; Nakashima et al., 2009). 이러한 결과를 통해 SnRK2.2, SnRK2.3, OST1 (SnRK2.6)과 같은 인산화효소들은 앱시스산 신호전달의 양성조절자(positive regulator)로서 기능을 한다는 것을 알 수 있다.
인산화효소와 함께 중요한 앱시스산의 신호전달자로서의 역할을 하는 것이 탈인산화효소다. 이 탈인산화효소 중 type 2C 탈인산화효소(PP2C)가 환경스트레스 및 앱시스산과 가장 연관이 되어 있다고 알려져 있다. 모델식물로 알려져 있는 애기장대(Arabidopsis thaliana)의 경우 76개의 PP2C가 존재한다고 알려져 있는데 이는 인간(15개)이나 효모(yeast, 7-9개)에 존재하는 PP2C에 비해 그 수가 현저히 많다(Schweighofer et al., 2004). 식물이 이렇게 많은 PP2C를 가지고 있는 것은 두 가지로 해석될 수 있다. 첫 번째로, 스트레스에 대해 회피를 할 수 없는 식물의 특성상 빠른 신호전달과정이 필요한데 양성조절자를 활성화 하는 것보다는 음성조절자들을 불활성화 시키는 반응이 훨씬 빠르게 일어나기 때문이다. 인산화효소의 경우 양성조절자로서 역할을 많이 하고 탈인산화효소의 경우 음성조절자로서 역할을 많이 하기 때문에 식물의 경우 탈인산화효소를 많이 가지고 있을 수 있다. 두 번째 이유로는 식물의 경우 동물보다 스트레스에 노출될 확률이 높기 때문에 각각의 스트레스를 조절하는 많은 탈인산화효소가 존재 할 수 있다는 것이다. 애기장대에서 PP2C는 10개의 그룹으로 나뉘어져 있는데 유전학적, 분자생물학적, 식물생리학적인 연구를 통하여 많은 식물의 PP2C 역할이 밝혀지고 있다. 이중에서 앱시스산에 의하여 발현이 유도되는 A group의 PP2C는 9개의 member로 구성되어 있는데 이중 6개의 PP2C가 앱시스산 신호전달과정에서 음성 조절자로 작용한다는 것이 밝혀졌다(Gosti et al., 1999; Merlot et al., 2001; Rubio et al., 2009; Wasilewska et al., 2008). 이들 유전자(ABI1, ABI2, HAB1, HAB2, AHG1, PP2CA)가 발현이 되지 않는 돌연변이체의 경우 앱시스산에 과민(hypersensite)한 반응을 보여 앱시스산이 첨가된 배지에서 발아가 억제되는 표현형을 보였다(Kuhn et al., 2006; Nishimura et al., 2004; Robert et al., 2006; Rubio et al., 2009; Saez et al., 2004, 2006; Yoshida et al., 2006b). 반면에 우성돌연변이체인 abi1-1, abi2-1의 경우 발아, 기공개폐에서 앱시스산에 둔감한 표현형을 보였다(Allen et al., 1999; Finkelstein and Somerville, 1990; Koornneef et al., 1984; Leung et al., 1997). 이 우성 돌연변이들은 단백질 탈인산화효소가 계속적으로 활성화되어서 앱시스산에 대하여 무감각하게 되고, 이것은 이 유전자들이 발현되지 못하거나 발현된 단백질이 기능을 하지 못하는 돌연변이체와 반대의 표현형을 보였다. A 그룹의 PP2C는 어느 정도의 특이성(specificity)과 중복성(redundancy)이 함께 기능을 하는데 각각의 돌연변이체가 표현형으로 나타나 우리가 인식할 수 있는 앱시스산의 과민성을 나타내는 반면에, 몇몇의 이중 돌연변이는 단일 돌연변이와 비교하여 앱시스산에 훨씬 큰 과민성을 보였다(Merlot et al., 2001; Rubio et al., 2009). 이러한 연구 결과통하여 A 그룹의 PP2C는 SnRK-2 type의 인산화효소와는 반대로 앱시스산의 음성조절자로서 역할을 한다고 말할 수 있다.
앱시스산 신호전달 과정에서 SnRK2 인산화효소와 PP2C 탈인산화효소의 상호작용
몇몇 연구들을 통하여 SnRK2 type 인산화효소와 A 그룹의 PP2C 탈인산화효소 사이의 기능적이고 물리적인 상호작용이 입증되었다. Yoshida 등(2006a)은 이러한 상호작용에 대하여 가장 먼저 제시를 하였는데 이는 A group PP2C 중 앱시스산의 음성조절자로서 그 기능이 가장 잘 알려져 있는 ABI1과 ABI2 단백질과 앱시스산의 양성조절자로서 그 기능이 가장 잘 알려져 있는 인산화효소인 SnRK2.6/OST1가 서로 상호작용을 한다는 것이다. 또한 최근의 연구를 통하여 앱시스산 신호전달에서 기능하는 몇몇의 SnRK2 type의 인산화효소와 PP2C 탈인산화효소간의 상호작용을 통하여 앱시스산의 신호전달 과정이 조절이 되는 것이 밝혀졌다(Fujii et al., 2009; Lee et al., 2009; Umezawa et al., 2009; Vlad et al., 2009; Yoshida et al., 2006a). 예를 들어, A 그룹의 PP2C의 경우 OST1과의 상호작용을 통하여 OST1의 자가인산화를 억제하고 또한 이 단백질의 기질인 공변세포의 SLAC1 음이온 채널의 인산화를 억제하는 역할을 하여 앱시스산에 의해 유도되는 기공의 개폐에 중요한 역할을 한다고 밝혀졌다(Geiger et al., 2009; Lee et al., 2009). PP2C와 OST1 사이의 물리적 상호작용은 OST1을 불활성화 시켜 기공 폐쇄에 작용하는 SLAC1 채널의 활성을 낮추고 앱시스산에 의해 유도되는 유전자 발현을 억제하는 역할을 한다고 알려졌다(Nishimura et al., 2010; Yoshida et al., 2006a). 또한 ABI1, PP2CA를 포함한 A 그룹의 PP2C가 탈인산화 효과 뿐만 아니라 단지 물리적 상호작용에 의해서 OST1을 불활성화 시킨다는 것이 밝혀 졌다. 이는 효소의 활성 뿐 아니라 상호작용 같은 다른 작용도 생물의 신호전달에 굉장히 중요한 역할을 한다는 것을 보여주는 것이며 여러 신호전달과저에서 인산화효소와 탈인산화효소의 상호작용에 대한 연구가 최근에 더 활발히 이루어 지고 있다(Fujii et al., 2009; Lee et al., 2009; Umezawa et al., 2009).
PP2C의 3중 돌연변이체(triple mutant)인 abi1-2/hab1-1/pp2ca-1에서 SnRK2 type의 인산화효소가 강한 활성을 나타내게 되는데 이는 PP2C의 활성이 결여되어 앱시스산 신호전달과정이 활성화 되어 일어난 것으로 추정된다(Fujii et al., 2009). Hubbard 등(2010)은 앱시스산 신호 전달경로에서 가장 빠른 과정들은 PYL/PYR/RCAR, PP2C 그리고 SnRK2 사이의 상호작용으로 이루어진다고 제안하였다. PP2C(음성 조절자)와 SnRK2(양성 조절자) 사이의 상호작용은 앱시스산 신호전달을 억제시킨다. PYL/PYR/RCAR과 PP2C의 앱시스산 의존적 그리고 종종 비의존적 결합은 PP2C의 SnRK2 불활성화를 억제시켜 SnRK2의 활성화와 앱시스산 신호전달경로의 활성화를 야기한다(Fujii et al., 2009; Lee et al., 2009; Ma et al., 2009; Park et al., 2009; Umezawa et al., 2009).
앱시스산 신호전달과정에서 이온 채널 및 기공 개폐 조절
앱시스산에 의해 조절되는 기공 개폐는 공변세포의 세포막과 액포막(tonoplast)에 위치하는 이온 채널의 조절과 연관되어 있다(Schroeder et al., 2001a). 식물이 건조 스트레스에 노출되었을 때 앱시스산이 여러 조직에서 생합성 되어 잎 조직 특히 공변세포에 축적이 된다. 이들 앱시스산의 경우 S-type 음이온 채널(SLAC1)과 밖으로 향하는(outward rectifying) K+채널을 활성화시키는 반면 안쪽으로 향하는(inward rectifying) K+채널은 불활성화 시켜 이온 이동이 바깥쪽으로 향하게 하고 이로 인하여 공변세포에서 수분의 손실이 일어나 공변세포의 팽압이 감소하게 된다(Kim et al., 2010; Nilson and Assmann 2007; Schroeder et al., 2001b; Ward et al., 2008; Wasilewska et al., 2008). 건조나 다른 스트레스 조건에서 앱시스산 수준이 증가하면, 음이온 채널을 통한 음이온의 유출은 탈분극(depolarization)을 유발하고 이는 공변세포에 스트레스로 작용을 하게 되어 이들 이온에 대한 평형을 맞추기 위해 바깥쪽으로 향하는 K+채널을 활성화시킨다(Kim et al., 2010; Ward et al., 2008). 공변세포 내에서 이온 농도가 감소되면 삼투현상에 의해 수분이 공변세포 바깥으로 유출되고 이는 공변 세포의 부피를 감소 시켜서 그에 따라 기공의 폐쇄를 유도하게 된다(Ward et al., 1995; Wasilewska et al., 2008).
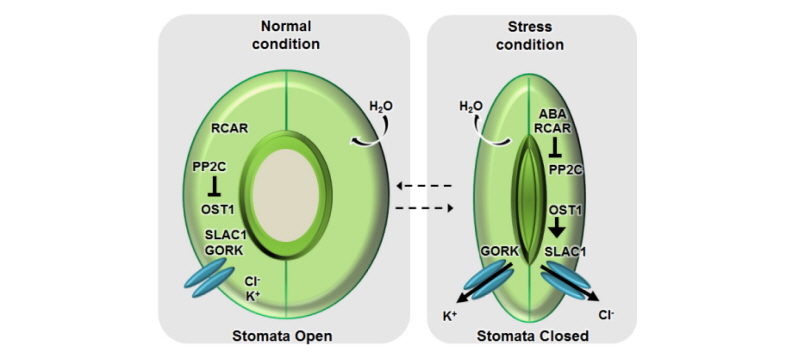
A 그룹 PP2C인 ABI1과 ABI2 그리고 SnRK2 type 인산화효소인 OST1/AAPK이 대표적으로 공변세포의 이온 채널활성과 관련되어 있다고 알려져 왔다(Li et al., 2000; Pei et al., 1997). 현재까지 앱시스산 신호전달을 설명한 여러 연구를 통하여 앱시스산 신호전달과정에서 유전자들의 발현, 이온 채널 조절 및 기공의 개폐 조절과 연관 된 모델이 Fig. 1에 제시되었다. 식물이 스트레스를 받지 않거나 낮과 같이 광합성이 활발하게 일어나는 상태에서는 식물 스트레스 호르몬인 앱시스산의 생합성이 많이 이루어지지 않아 세포에서 앱시스산을 인식하는 수용체인 PYR/ PYL/RCAR 단백질의 수준도 낮게 유지가 된다. 이 상태에서는 A 그룹 PP2C는 SnRK2 type 인산화효소와 결합하고 있으며 인산화효소의 활성을 방해한다. 또한 SLAC1과 같은 음이온 채널들과 GORK (guard cell outward rectifying potassium channel)가 탈인산화 되어 활성이 낮게 유지된다. 그러나 건조와 같은 스트레스 요인이 발생을 하게 되면 식물은 이에 반응하여 앱시스산이 생합성 되고 이 생합성 된 앱시스산은 공변세포에서 PYR/PYL/RCAR 수용체와 결합을 하게 된다. 앱시스산과 결합이 된 PYR/PYL/RCAR는 PP2C와 상호작용을 하게 되고 이는 SnRK2와 PP2C의 상호작용을 방해하게 되어 SnRK2의 인산화작용 활성화를 유도하게 된다. 결과적으로 SLAC1 및 다른 채널들을 인산화시켜 채널을 활성화 시키고 이온들을 유출하게 한다. 이것은 삼투로 인한 공변세포에서의 수분 유출을 유도하고 공변세포의 팽압을 낮추어 기공의 폐쇄를 유도 한다(Geiger et al., 2009, 2010; Lee et al., 2009; Pei et al., 1997).
결 론
식물의 대표적 호르몬 중 하나인 앱시스산은 종자의 휴면, 식물 생장 및 발달, 스트레스에 대한 반응을 조절하는 복잡한 신호전달 네트워크를 활성화 시킨다. 복잡한 신호전달 과정들 사이의 상호작용을 정확하게 분석하기는 어렵지만 앱시스산에 의한 기공의 폐쇄가 스트레스에 대한 주요한 반응임은 확실하다. 한편으로는 기공의 폐쇄가 건조 같은 무생물적 스트레스에 반응하여 수분을 보존하는 역할을 하고, 다른 한편으로는 닫힌 기공이 병원균의 침투에 대한 방어 장벽으로 작용한다. 이들 경우에서, 앱시스산 신호전달과정은 세포의 반응에서 신호를 통합하는 역할을 한다는 것을 알 수 있었다. 최근의 연구에서 앱시스산이 환경스트레스 내성에 기능하는 분자 수준의 신호전달 기작에서 다양한 역할을 한다는 것이 밝혀졌다. PYR/PYL/RCAR, PP2C, SnRK2 그리고 SLAC1 채널 등의 앱시스산 신호전달에서의 분자적 구성요소는 스트레스에 대해 내성을 갖는 작물을 유전적으로 조작하는 데에 유용한 유전자원이 될 수 있다. 하지만 이들 신호전달 과정의 복잡성은 앞으로 풀어나가야 하는 숙제로 남아있다. 예를 들어, 앱시스산 신호전달과 관련된 14개의 PYR/PYL/RCAR 수용체, 6-9개의 A type PP2C, 그리고 최소한 3개의 SnRK2 인산화효소가 있고 이들의 상호작용 및 여러 효소로서의 기능을 밝히는 것은 앱시스산 신호전달과정을 연구하는 데 중요한 과제이다. 따라서 PYL/RCAR-PP2C-SnRK2 복합체의 경우 200개 이상의 가능한 조합이 존재 한다. 각각의 조합은 세포의 유형, 앱시스산의 농도 그리고 세포 내에서의 위치에 따라 동일하거나 다른 하위(downstream) 단계에서의 목표를 조절할 것이고, 미세한 조정의 거대한 복잡성을 가진다. 이 신호전달 경로의 미세 조정에 관한 앞으로의 연구는 우리가 스트레스 반응간의 상호작용을 이해하는데 도움이 될 것이다.