서 론
재료 및 방법
실험재료
차가버섯의 로스팅 및 시료 제작
세포 배양 및 분화
세포독성 평가
세포내 지방축적량 확인
지방분화 관련 단백질 발현량 분석
통계처리
결과 및 고찰
로스팅 차가버섯 추출분말의 세포독성 확인
분화가 유도된 3T3-L1 세포에서 로스팅 차가버섯 추출분말의 지방구 억제 효과
로스팅 차가버섯 추출분말의 처리에 따른 지방분화 관련 단백질 분석
요 약
서 론
비만은 전 세계적에서 가장 빠르게 증가되고 있는 심각한 공중보건 문제 중 하나로서, 심혈관 질환, 제2형 당뇨병, 대사성 질환과 특정 암의 발생과 밀접한 관련이 있는 것으로 알려져 있고, 특히 내장지방형 비만 같은 경우 인슐린 저항성이나 내당능 장애, 고혈압, 그리고 이상지질혈증 등을 유발하는 중요한 위험요소인자로 보고되고 있다(Joo et al., 2010; Nakamura et al., 1994). 따라서 이러한 비만을 사전에 미리 예방하고 비만과 관련되어 있는 질환들을 예방 및 치료하기 위하여 다양한 예방제나 치료제가 개발되어 있는데, 아직까지 독성 및 부작용이 끊임없이 제기되고 있으므로 이를 보완하기 위하여 여러 가지 생리활성 물질을 함유하고 있는 천연물들이 후보군으로 꾸준하게 제시되고 있는 실정이다(Joo et al., 2010). 최근 들어 평균수명이 크게 증가하면서 삶의 질에 대한 인식의 변화로 인하여 운동요법이나 식이요법들이 각광받고 있으며, 이외에도 체중 조절에 효과적인 기능성 원료, 특히 식물성 화합물인 파이토케이칼(phytochemical)을 이용한 항 비만 활성 검증과 그 작용 기전을 이해하고자 하는 연구들이 계속되고 있다(Kang et al., 2007; Kang et al., 2008; Mercader et al., 2011; Perez-Vizcaino et al., 2006; Rayalam et al., 2008). 이러한 파이토케이칼은 과일이나 야채 같은 과채류 등에 많이 포함되어 있으며 비영양 성분들로 항산화, 항염, 항암 등의 생리활성에 효능이 있다고 알려져 있고, 항비만과 관련하여 지방세포의 세포주기를 조절하여 관련 단백질 및 유전자의 발현을 조절하는 것으로 보고되고 있다(Eberhardt et al., 2005; Khor et al., 2008; Lim et al., 2012).
담자균류(Basidiomycota)의 민주금버섯목(Aphyllophorales), 소나무비늘버섯과(Hymenochaetaceae), 시루뻔버섯속(Inonotus)에 속하는 차가버섯(Inonotus obliquus (Pers.) Pilot)은 한랭 다습한 북반구의 자작나무, 오리나무, 마가목에서 자생하는 버섯으로 주로 러시아의 시베리아나 핀란드, 노르웨이 같은 북유럽 등지에서 주로 자생하며 일부 국내 오대산 등지에서 자생하고 있다고 보고되어 있다(Guk et al., 2013; Shashkina et al., 2006). 차가버섯은 최적의 자생환경을 가지고 있는 러시아에서 1950년대 말부터 연구가 시작되어 차가버섯의 자실체에서 추출한 β-glucan, polyphenol 및 polysaccharides, peptides, triterpenoids, steroids 등 다양한 기능성 성분들을 함유하고 있다고 알려져 있다(Cui et al., 2005; Guk et al., 2013; Hyun et al., 2006; Lee et al., 2007; Nakajima et al., 2007; Rhee et al., 2008; Shashkina et al., 2006; Zhang et al., 2007).
이러한 차가버섯과 관련된 연구들을 살펴보면, 차가버섯 추출물이 산화스트레스 예방이나 항염, 통증완화 등에 효과가 있다고 보고되어 있으며, 특히 흑색종 세포 B16-F10, 대장암 세포 DLD-1, 자궁경부암 세 포 HeLa S3 그리고 위암세포 SNU-484 등 다양한 암 세포주의 증식을 억제하며 뛰어난 항암효과를 보이는 것으로 연구되어 있어 많은 암 환자들에게 각광받고 있다(Burczyk et al., 1996; Hwang et al., 2003; Kim et al., 2006; Kim et al., 2007; Lee et al., 2007; Najafzadeh et al., 2007; Park et al., 2005; Sung et al., 2008; Youn et al., 2009). 하지만 항비만과 관련된 연구결과는 미비한 상황이다.
따라서 본 연구에서는 차가버섯 원물과 3가지 다른 조건으로 로스팅한 차가버섯을 이용하여 분화된 3T3-L1 지방세포에 처리하였을 때 지방구 축적이나 지질대사 관련 유전자 발현에 영향을 미치는지 규명하고자 하였다.
재료 및 방법
실험재료
차가버섯은 ㈜아르뜨라이프사(Russia)에서 원물을 구입하였으며, 지방전구세포(3T3-L1)는 Lonza (Switzerland)에서 구입하여 사용하였다. 지방전구세포의 배양에 필요한 배지와 Penicillin-streptomycin은 Thermofisher (USA)에서 구입하였으며, 분화에 사용되는 insulin, dexamethasone (DEX), 3-isobutyl-1-methylxanthine (IBMX), nitroblue tetrazolium (NBT), Oil red O (ORO), isopropyl alcohol, N-acetyl-L-cystein (NAC), tetrazolium salt (MTT) 및 기타 시약들은 Sigma-Aldrich (USA)에서 구입하여 사용하였다.
차가버섯의 로스팅 및 시료 제작
차가버섯의 로스팅은 디지털 로스터기인 SMART 1500 (IMEX Corporation Ltd, Korea)을 이용하여 진행하였으며, 시즈히터를 이용하여 3가지 조건하에서 로스팅을 수행하였다(Table 1).
Table 1. Roasting conditions of Inonotus obliquus 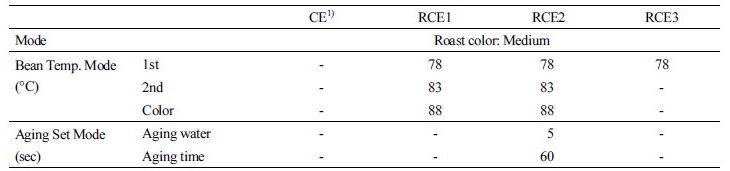 | |
1)CE, Inonocus obliquus extract; RCE1, roasted I. obliquus extract 1; RCE2, roasted I. obliquus extract 2; RCE3, roasted I. obliquus extract 3. | |
대조군으로 사용할 차가버섯 원물과 로스팅 차가버섯을 준비하고 증류수에 침지시켜 70°C에서 24시간 동안 추출하였으며, 완성된 추출액을 filter papter (Whatman paper No. 2)를 사용하여 감압여과장치로 여과 및 분리하고 대형 회전농축기로 70°C water bath에서 60 rpm의 속도로 최전시키며 감압농축을 실시하였다. 완성된 농축액은 deep freezer에서 24시간 동안 냉동시킨 후 동결건조기에서 3일 이상 차가버섯 시료의 분말화를 위한 동결건조를 진행하였으며, 동결건조가 끝난 후 시료를 분쇄하여 냉동보관하고 실험에 사용하였다.
세포 배양 및 분화
지방전구세포인 3T3-L1은 10% Bovine Calf Serum (BCS, Welgene, Korea) 및 1% penicillin-streptomycin이 포함된 Dulbecco's modified Eagle's media를 사용하여 37°C, 5% CO2의 조건에서 배양하였다. 배양개시 2일 후 3T3-L1 지방전구세포를 지방세포 분화유도 물질 (10 ug/mL insulin, 1 uM DEX, 0.5 mM IBMX)과 FBS (10%) 및 P/S (1%)를 함유한 DMEM (분화배지)로 교환하여 2일간 추가 배양하였다. 그 후 분화배지로 교환하여 12일간 배양하면서 지방세포로의 분화를 유도하였다. 시료는 2일마다 지방세포 분화 유도 기간 동안 배양액에 처리하였다.
세포독성 평가
생세포의 미토콘드리아에서 탈수소 효소작용에 의해 노란색의 MTT tetrazolium을 청자색의 비수용성 MTT formazan (3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyl-tetrazolium bromide)으로 환원시키는 능력을 이용하여 세포독성을 측정하였다(Carmichael et al., 1987; Mosmann, 1983). 지방전구세포인 3T3-L1을 24-well plate에 2 × 104/well로 분주하여 5% CO2, 37°C 배양기에서 전배양하였으며, 차가버섯 추출분말을 농도별(0-200 ug/mL)로 처리하여 전배양 조건과 동일한 환경에서 24시간 배양하였다. 배양종료 4시간 전 MTT solution (5 mg/mL)을 첨가하여 반응시킨 후 배지를 제거하고 DMSO로 용해하였으며, spectrophotometer를 이용하여 570 nm에서 흡광도를 측정하였다.
세포내 지방축적량 확인
분화과정에 따른 3T3-L1 세포내 지방축적량을 확인하기 위하여 각각의 시료를 처리한 6-well 에서 12일 동안 분화된 3T3-L1 세포의 배양액을 제거한 후, 10% formalin 1 mL를 첨가하여 5분간 실온에서 방치하였다. 이후 동량의 10% formalin 용액을 다시 첨가하고 분화된 세포를 1시간 이상 실온에서 방치한 후 상등액을 제거하고 60% isopropanol 500 uL를 첨가하여 세포를 세척한 후 완전히 건조시켰다. Oil red O working solution (Oil red O: 멸균증류수 = 6 : 4)으로 세포 내에 축적된 지방성분들을 염색한 후 PBS (phosphate buffered saline, pH 7.4)를 사용하여 3-5회 이상 세척하여 용액을 완전히 제거한 후 핵 염색을 위하여 hematoxylin을 1분간 처리하였다. 이후 세척하여 hematoxylin을 완전히 제거하고 건조시킨 후 이미지를 촬영하고, 지방성분과 결합한 Oil red O 성분을 100% isopropanol로 용해시켜 520 nm에서 흡광도를 측정하였다.
지방분화 관련 단백질 발현량 분석
지방조직에서 주로 확인되며 세포 분화에 영향을 미치는 peroxisome proliferator-activated receptor gamma (PPAR-γ)와 CCAAT/enhancer binding protein alpha (C/EBP-α) 단백질의 발현양을 측정하기 위하여 Western blot analysis를 수행하였다. 배양된 세포의 배지를 제거한 후 RIPA buffer로 lysis 시키고 cell scraper를 이용하여 세포를 회수하고 BCA법으로 단백질을 정량한 후, 10% SDS gel을 이용하여 30 ug의 단백질을 전기영동하였다. 이후 PVDF membrane에 전이하여 blocking - 1stantibody-2ndantibody의 순서대로 배양하고, WEST-ZOL Plus를 이용하여 화학발광염색방법으로 단백질의 발현정도를 확인하였다.
통계처리
모든 측정은 3회 반복하였으며 측정값의 통계처리는 Student’s t-test를 이용하여 평균과 표준편차로 나타내었다.일원배치 분산분석(one-way ANOVA)을 이용하여 분석하였으며, p<0.05 인 것을 유의적인 결과로 판단하였다.
결과 및 고찰
로스팅 차가버섯 추출분말의 세포독성 확인
지방전구세포인 3T3-L1에서 로스팅 차가버섯 추출분말의 세포독성이 있는지 확인하기 위하여 MTT 법으로 세포독성율을 확인하였다(Park et al., 2013). 그 결과, 로스팅을 하지 않은 차가버섯 추출분말인 CE (Chaga Extract)에서는 20-200 ug/mL 농도에서는 세포독성이 나타나지 않았고, 서로 다른 조건에서 로스팅한 차가버섯 추출분말 가운데 RCE (Roasted Chaga Extract) 1, RCE 2 의 경우에는 150-200 ug/mL 수준에서 대조군과 비교하여 약간의 감소현상을 보였으나, 유의적인 차이는 나타내지 않았다(Fig. 1A-C). 반면에, 단시간에 로스팅을 수행한 차가버섯 추출분말인 RCE (Roasted Chaga Extract) 3는 20-100 ug/mL 농도에서는 대조군과 유사하였으나, 150, 200 ug/mL 처리 시 유의적으로 세포의 생존율이 감소하여 세포독성이 있는 것으로 나타났다(Fig. 1D).
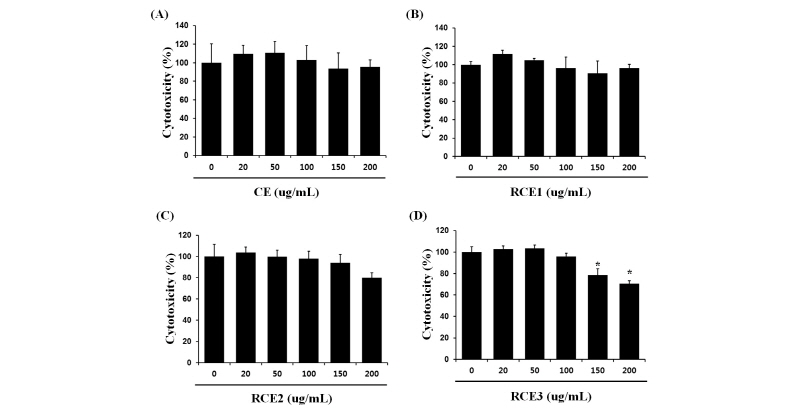
Fig. 1.
The cytotoxic effect of Inonotus obliquus extract (A) and the extracts according to each roasting condition (B, C, D). Cell viability was measured by MTT assay. 3T3-L1 preadipocytes were incubated with extracts of I. obliquus (CE, Chaga Extract) and roasted I. obliquus (RCE1, RCE2, RCE3, Roasted Chaga Extract) at various concentrations (0, 20, 50, 100, 150, and 200 ug/mL) for 24 h. The data shown in the graphs are the mean ± SD (n≥3). *P < 0.01 versus control.
분화가 유도된 3T3-L1 세포에서 로스팅 차가버섯 추출분말의 지방구 억제 효과
지방전구세포인 3T3-L1을 12일 동안 분화시킨 후 Oil red O staining을 통해 세포내 지방구(Lipid droplet) 생성을 확인한 결과, 시료를 처리하지 않고 분화한 세포 대조군과 비교하여 CE, RCE 1, RCE 2, RCE 3을 각각 100, 200 ug/mL 처리하였을 때 모두 큰 폭으로 지방구 형성이 감소되는 것을 확인하였으며, 이와 같은 경향은 음성 대조군으로 사용한 NAC (N-Acetyl choline)보다 더 큰 폭의 유의적인 감소 효과를 나타냈다(Fig. 2). 그리고 농도별로 보면, 각각의 추출물을 100, 200 ug/mL로 처리한 지방세포에서 지방구의 형성 억제가 200 ug/mL을 처리하였을 때 더 효과적인 것을 확인하였다. 또한, 차가버섯 원물 추출물과 로스팅 차가버섯 추출물을 비교한 결과 차가버섯 원물 추출물인 CE에 비해 로스팅 조건별 차가버섯 추물인 RCE 1, RCE 2, RCE 3을 분화된 지방세포에 100 ug/mL 처리할 경우 모두 지방구 억제가 더 활발히 일어나는 것을 확인하였으며, 200 ug/mL을 처리한 경우에는 RCE 1에서 가장 크게 억제 효과를 보였다. 전체적으로 보면, 분화가 유도된 지방세포의 대조군에 비해 RCE 1을 200 ug/mL 처리했을 때 가장 지방구 억제가 유의적인 수준으로 나타났으며 이는 차가원물 추출물인 CE와 비교했을 때에는 유의적인 수준으로 감소되었다.
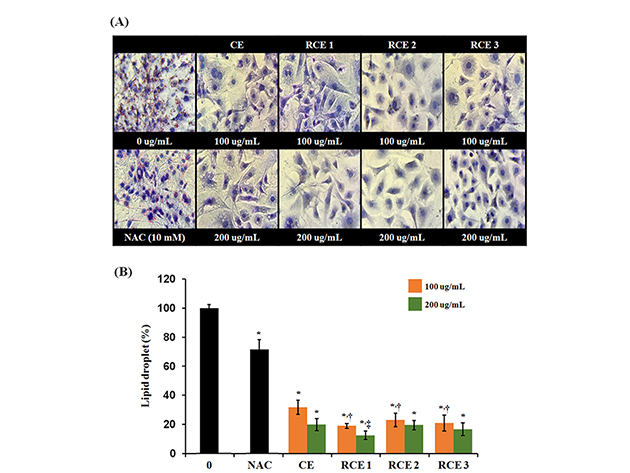
Fig. 2.
Inhibitory effect of Inonotus obliquus and roasted I. obliquus extracts on lipid accumulation in 3T3-L1 adipocytes. 3T3-L1 cells differentiated with differentiation media in the I. obliquus (CE, Chaga Extract), roasted I. obliquus extracts (RCE1, RCE2, RCE3, Roasted Chaga Extract, 100 and 200 ug/mL), and NAC (N-acetyl-L-cystein, negative nontrol) for 12 days. The data shown in graphs are the mean ± SD (n≥3). *P < 0.01 versus control, †P < 0.01 versus I. obliquus extracts (100 ug/mL), ‡P < 0.01 versus I. obliquus extracts (200 ug/mL).
로스팅 차가버섯 추출분말의 처리에 따른 지방분화 관련 단백질 분석
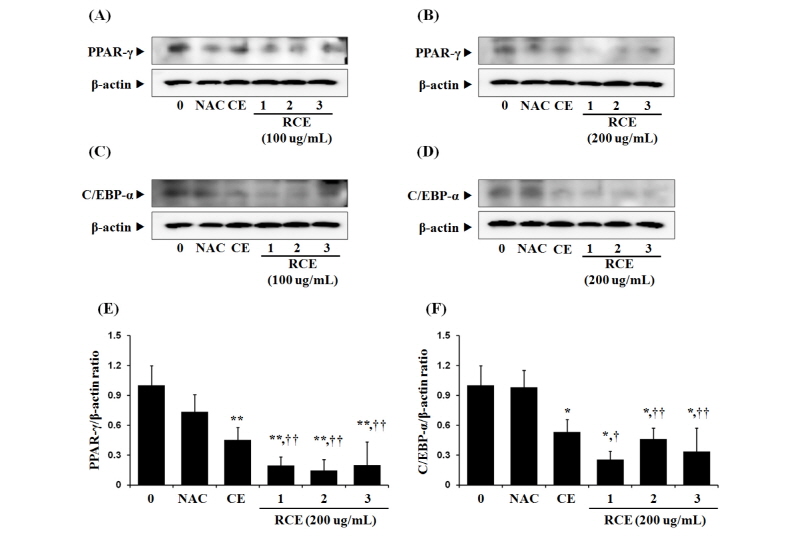
지방세포는 지방전구세포를 거쳐 지방세포로 분화되며, 그 과정에서 etinoid X receptor (RXR)와 heterodimer를 형성하여 표적물질의 발현을 조절하는 단백질인 PPAR-γ (Peroxisome proliferator-activated receptor gamma)와 Basic leucine zipper 군에 속하는 전사인자로써 초기 지방세포 분화에 관여한다고 알려져 있는 C/EBP-α (CCAAT enhancer binding protein α)가 영향을 미치게 된다(Gesta et al., 2007; Park et al., 2013). 따라서 지방전구세포인 3T3-L1의 분화 과정에서 발현되는 지방분화 유도단백질인 PPAR-γ와 C/EBP-α의 발현 정도를 Western blot을 이용하여 측정하였다. 전구지방세포인 3T3-L1의 분화유도 과정에서 차가바섯 원물(CE) 및 로스팅 차가버섯 추출물(RCE 1, RCE 2, RCE 3)을 100, 200 ug/mL의 농도로 처리하고 PPAR-γ의 단백질 발현량을 확인한 결과, 지방분화로 증가한 PPAR-γ의 발현량이 RCE 1, RCE 2, RCE 3을 100, 200 ug/mL처리한 군 모두에서 감소하였으며, 특히 RCE 1, 2을 200 ug/mL 처리한 군에서 유의적 수준으로 억제되는 것을 확인하였다(Fig. 3A-B, E). 초기 지방세포 분화에 관여하는 C/EBP-α의 발현량을 확인한 결과, 분화 시 증가한 C/EBP-α 발현량이 CE와 RCE 1, RCE 2, RCE 3 모두에서 유의적 수준으로 감소하였으며, 그 경향을 200 ug/mL을 처리하였을 경우 유의적 수준으로 더욱 크게 나타났다(Fig. 3C-D,F). 이러한 결과를 바탕으로 차가버섯 추출물은 지방분화와 관련된 단백질 발현량을 조절할 뿐 아니라, 로스팅 과정을 통해 지방분화 관련 단백질의 발현량 억제 효과를 극대화한다는 것을 알 수 있었다.
Fig. 3.
Effect of Inonotus obliquus and roasted I. obliquus extracts on expression of PPAR-γ(A, B, E) and C/EBP-α(C, D, F). 3T3-L1 cells were differentiated with differentiation media containing extracts of I. obliquus (CE, Chaga Extract), roasted I. obliquus (100 and 200 ug/mL), and NAC(N-acetyl-L-cystein, negative control) for 12 days. The levels of PPAR-γ and C/EBP-α were determined by western blotting using specific antibodies. The protein expression ratio was calculated against β-actin and represented as arbitrary units of integrated density value. The data shown in the graphs are the mean ± SD (n≥3). **P < 0.05 and *P < 0.01 versus control, ††P < 0.05 and †P < 0.01 versus I. obliquus extracts (200 ug/mL) (Continued).
요 약
본 연구에서는 로스팅에 따른 차가버섯의 항비만 기능성 증진 효과를 확인하기 위하여 서로 다른 조건에서 차가버섯을 로스팅하고 그 추출분말을 제작한 후 지방전구세포인 3T3-L1의 세포독성을 확인하고 분화된 지방세포에서 지방구 축적 정도와 지방세포 분화와 관련된 단백질의 발현을 조사하였다. 결과에서 보는 것처럼, 지방전구세포인 3T3-L1에서 차가버섯 원물 추출물과 3가지 조건으로 로스팅한 차가버섯 추출물을 가지고 세포독성을 확인한 결과, 로스팅 조건 3번의 차가버섯 추출물을 150, 200 ug/mL을 처리하였을 때 세포생존율이 유의적으로 감소한 것을 제외하면 다른 모든 추출물에서는 유의적인 세포독성은 나타내지 않았다. 또한, Oil Red O 염색법을 통해 지방 축적량을 확인한 결과 차가버섯 원물 및 로스팅 차가버섯 추출물 모두에서 지방구 축적이 대조군에 비해 유의적으로 감소하였으며, 특히 로스팅 조건 2번의 차가버섯 추출물을 200 ug/mL로 처리한 경우에는 억제효과가 더욱 크게 나타났다. 마지막으로 Western blot analysis를 이용하여 지방분화 유도 단백질인 PPAR-γ와 C/EBP-α의 발현량을 확인한 결과, 차가버섯 원물 추출물보다는 조건별로 로스팅한 차가버섯 추출물 모두에서 PPAR-γ와 C/EBP-α의 발현량이 감소하였으며, 특히 100 ug/mL보다 200 ug/mL을 처리하였을 때 발현량이 더욱 감소되었다. 이러한 결과를 통해 차가버섯, 특히 로스팅한 차가버섯이 비만을 예방하는 잠재적 후보군으로서의 가능성 높다는 것을 확인할 수 있었다.